Klíčový rozdíl: Atomy jsou základní jednotky, ze kterých se všechny věci skládají. Atomy různých prvků spojují molekuly. To se děje prostřednictvím chemické reakce. Molekula je nejmenší množství chemické látky, která může existovat. V podstatě je sloučenina typ molekuly. Molekula může být tvořena dvěma nebo více atomy stejného prvku nebo dva nebo více atomů různých prvků. Nicméně sloučeniny jsou molekuly, které jsou tvořeny atomy různých molekul.
Prvek je čistá chemická látka, která má jeden nebo jeden typ atomu, který se vyznačuje svým atomovým číslem. Atomové číslo je odvozeno z počtu protonů přítomných v jádře prvku. Celkem bylo zjištěno 118 prvků, rozdělených mezi kovy, metaloidy a nekovy. Každý prvek má vlastní sadu vlastností. Většina prvků je k dispozici na zemi, zatímco některé byly uměle vytvořeny prostřednictvím jaderných reakcí. Prvek je již ve své nejsilnější podobě a nemůže být dále rozdělen. Všechny prvky lze nalézt v periodické tabulce, která je uvedena podle atomového čísla.
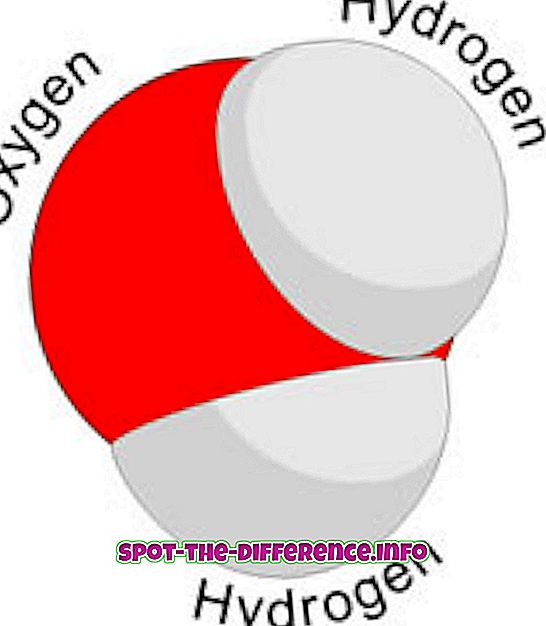
Atomy různých prvků spojují molekuly. To se děje prostřednictvím chemické reakce. Například: dva vodíkové atomy a jeden atom kyslíku se spojují, aby se vytvořila molekula vody.
Molekula je nejmenší množství chemické látky, která může existovat. Nejmenší množství vody, jakou může být, je molekula vody nebo H20. Je vyrobena z různých atomů společně; proto může být oddělena zpět do různých atomů.
Molekula může mít velmi odlišné vlastnosti od prvků, ze kterých je vyrobena. Například: voda se chová velmi odlišně než kyslík nebo vodík, i když je složena ze dvou atomů vodíku a jednoho atomu kyslíku.
Kromě toho nemůže atom existovat nezávisle v přírodě, aniž by se na ně něco spojil. Nikdy nenajdeme jen jediný atom kyslíku nebo jediný atom uhlíku. Je vždy spojen s něčím, jako je O2 (kyslík) nebo CO2 (oxid uhličitý). Když je molekula vázána do molekuly, může existovat nezávisle v přírodě, a proto můžeme vždy najít molekulu kyslíku, molekulu oxidu uhličitého, molekulu vody (H2O) atd.

Molekuly mají vždy sklon se seskupovat, jejich formování závisí na jejich stavu. Například v plynném stavu, molekuly mají tendenci být jen létání kolem. V kapalném stavu mají molekuly tendenci být volně seskupeny tak, aby se mohly stále pohybovat. Zatímco v pevném stavu jsou molekuly pevně zabaleny a mohou pouze vibrovat.
Molekuly jsou obvykle zastoupeny v molekulárním vzorci. Například: O2, H2O, CO2, C6H12O6 (cukr). Molekulární vzorec je název prvku, po němž následuje počet atomů tohoto prvku v molekule.
V podstatě je sloučenina typ molekuly. Molekula může být tvořena dvěma nebo více atomy stejného prvku nebo dva nebo více atomů různých prvků. Sloučeniny jsou však molekuly, které jsou tvořeny atomy různých prvků. Proto lze říci, že všechny sloučeniny jsou molekuly, avšak ne všechny molekuly jsou sloučeniny.
Proto jsou všechny molekuly vodík (H2), kyslík (02), dusík (N2), voda (H2O), oxid uhličitý (CO2) a metan (CH4). Pouze voda (H2O), oxid uhličitý (CO2) a metan (CH4) jsou však sloučeniny, ostatní nejsou.