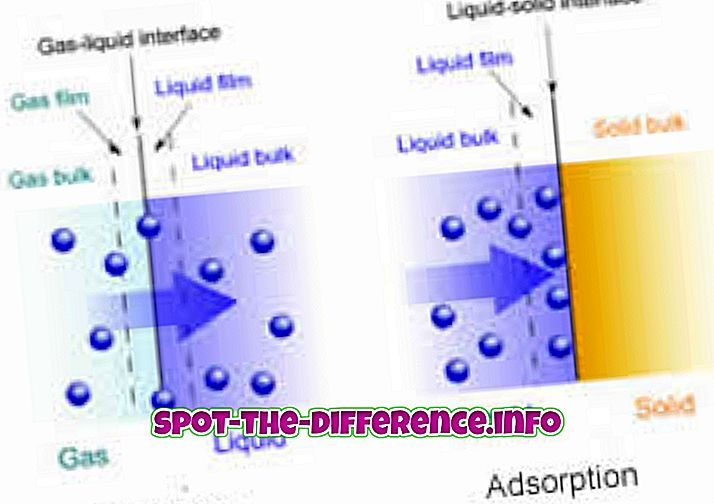
Klíčový rozdíl: Absorpce je hromadný jev, při kterém absorbent úplně proniká do těla pevného nebo kapalného za vzniku sloučeniny nebo roztoku. Na druhé straně adsorpce je povrchový jev, ve kterém se molekuly adsorbátu koncentrují pouze na povrchu adsorbentu.
Chemická reakce - oxid uhličitý absorbovaný roztokem uhličitanu draselného
Fyzikální proces - Vzduch absorbovaný ve vodě rozpuštěním

Existují dva typy režimů adsorpce - chemické a fyzikální. Při chemické adsorpci jsou molekuly a povrch spojeny slabými silami Vander Walls. Na druhé straně se v chemické adsorpci vytváří chemická vazba mezi molekulami a povrchem.
Primární rozdíl mezi adsorpcí a absorpcí proto spočívá v tom, že absorpce je velkým fenoménem, což znamená, že se to děje v celém těle materiálu, zatímco adsorpce zůstává povrchovým jevem. Adsorpce je vždy exotermní, zatímco absorpce je endotermická. Sorpce zahrnuje jak proces absorpce, tak adsorpci.
Srovnání adsorpce a absorpce:
Adsorpce | Vstřebávání | |
Definice | Akumulace plynné nebo kapalné látky na povrchu pevné látky nebo kapaliny | Difúze látky do kapaliny nebo pevné látky za vzniku roztoku nebo sloučeniny |
Příklad | Inertní plyny se adsorbují na dřevěném uhlí. | Suchá houba pohlcuje vodu |
Výměna tepla | Exotermní s výjimkou adsorpce H2 na skle | Endotermní |
Dosažení rovnováhy | Srovnatelně rychlejší | Srovnatelně pomalu |
Koncentrace | Koncentrace na povrchu adsorbentu se liší od objemu adsorbentu | Koncentrace zůstává stejná v celém materiálu |
Míra výskytu | Je to počáteční, ale později její míra začíná klesat | Probíhá s jednotnou sazbou |